수업후기
본 노트의 내용은
2017년 11월 5일 서울교대 전산교육관 101호 교육공학실에서 진행된
제9회 특별한 뇌과학 제 7강 (꿈과 기억)의 내용을 녹취한 것입니다.
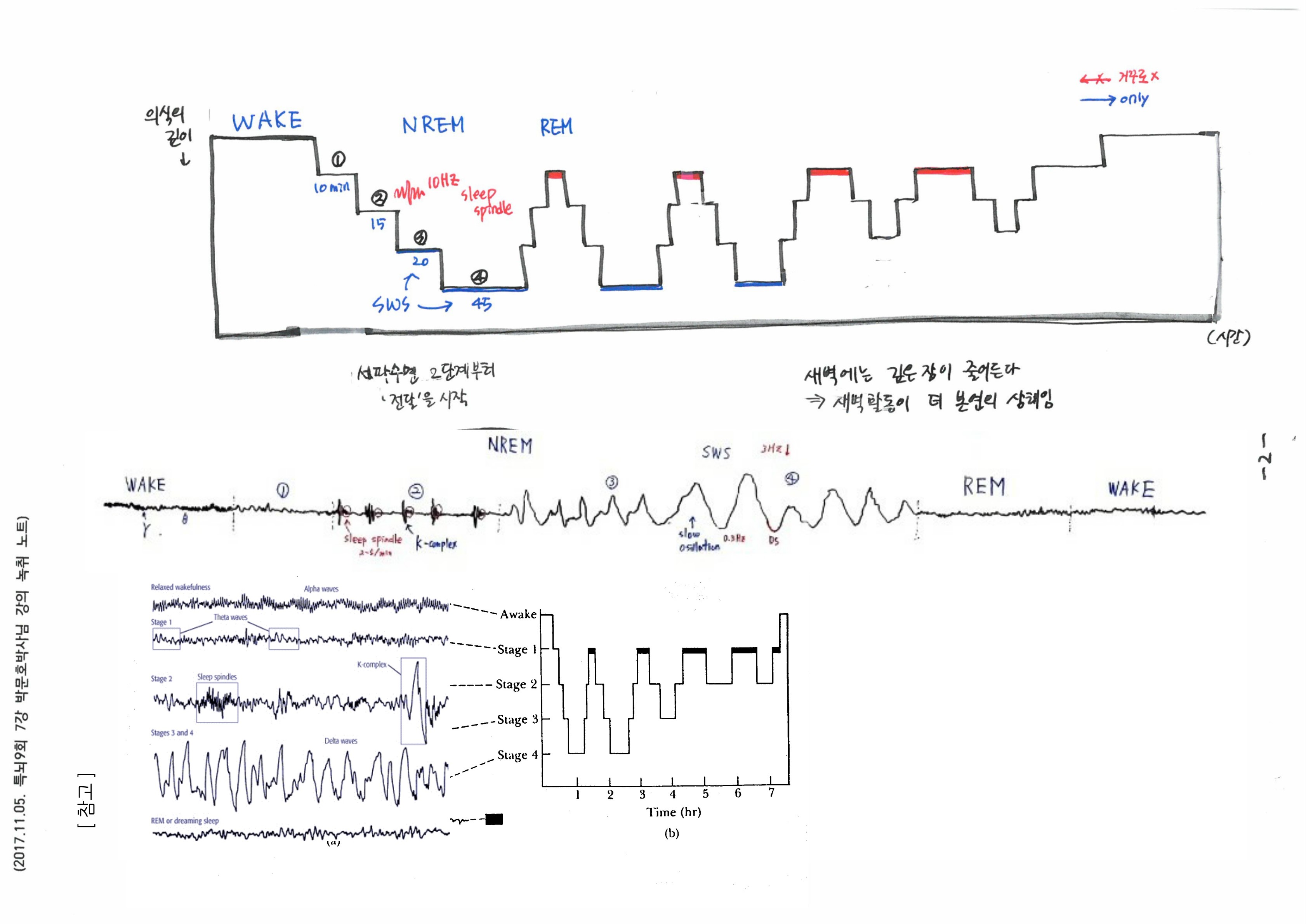
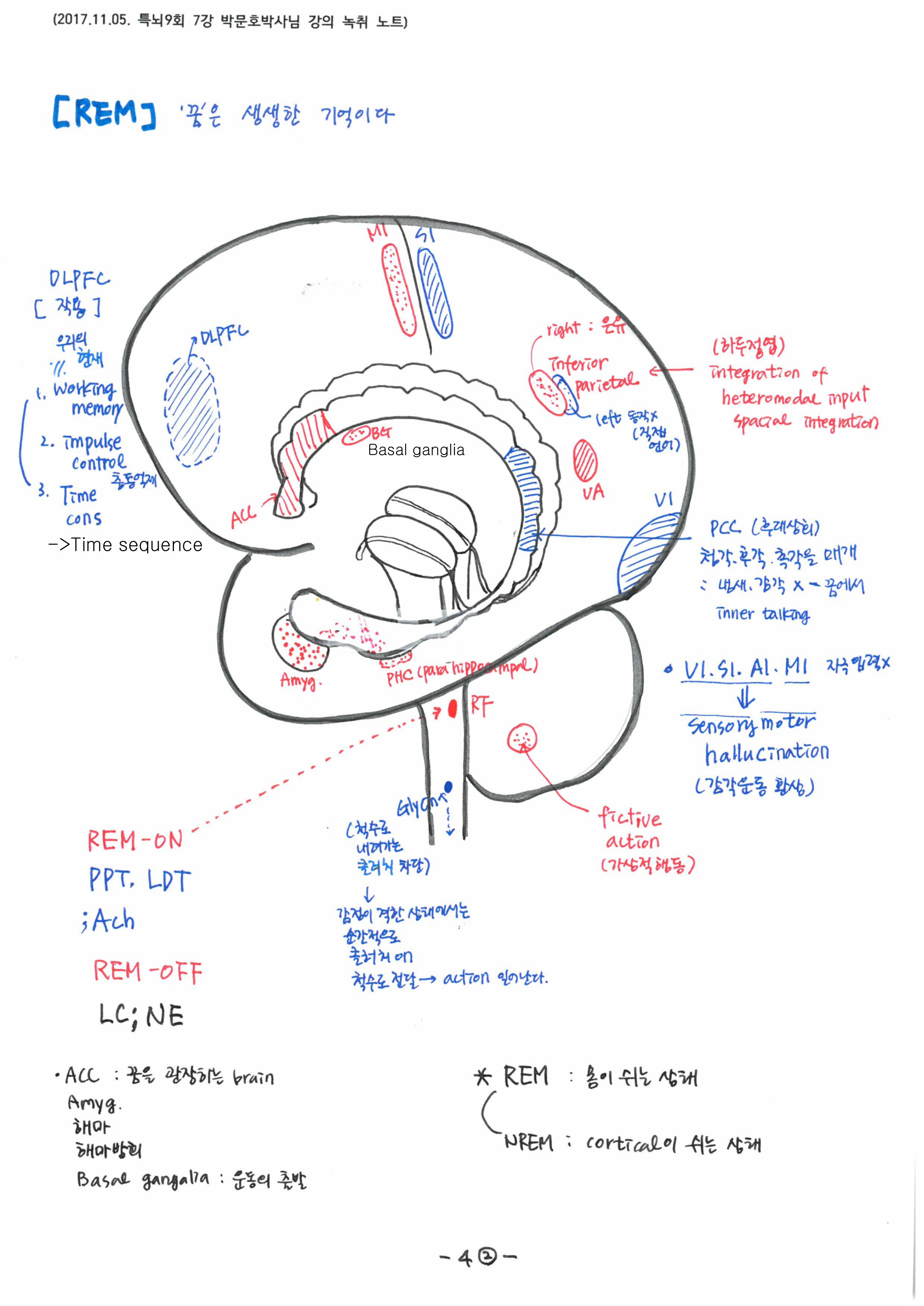
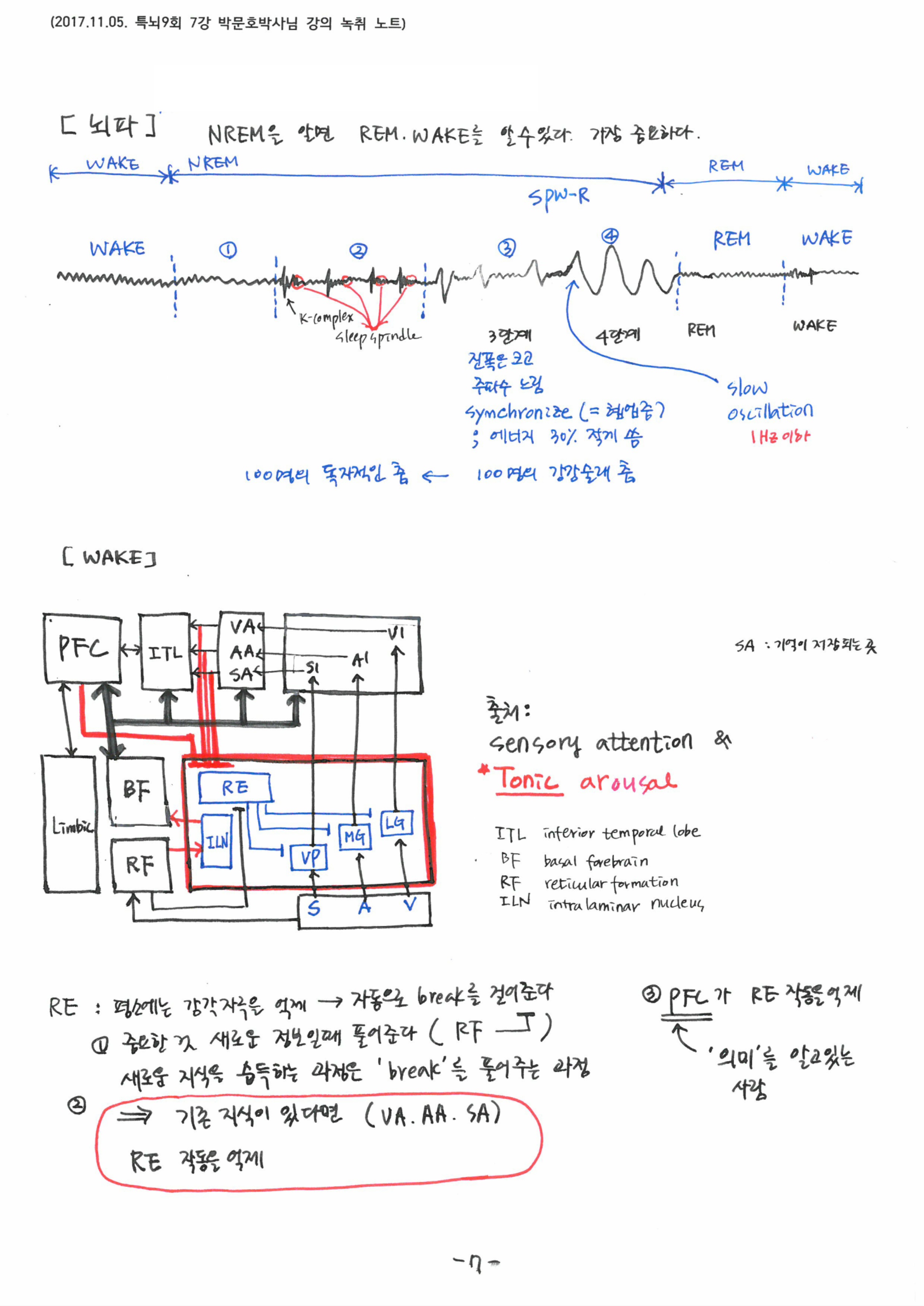
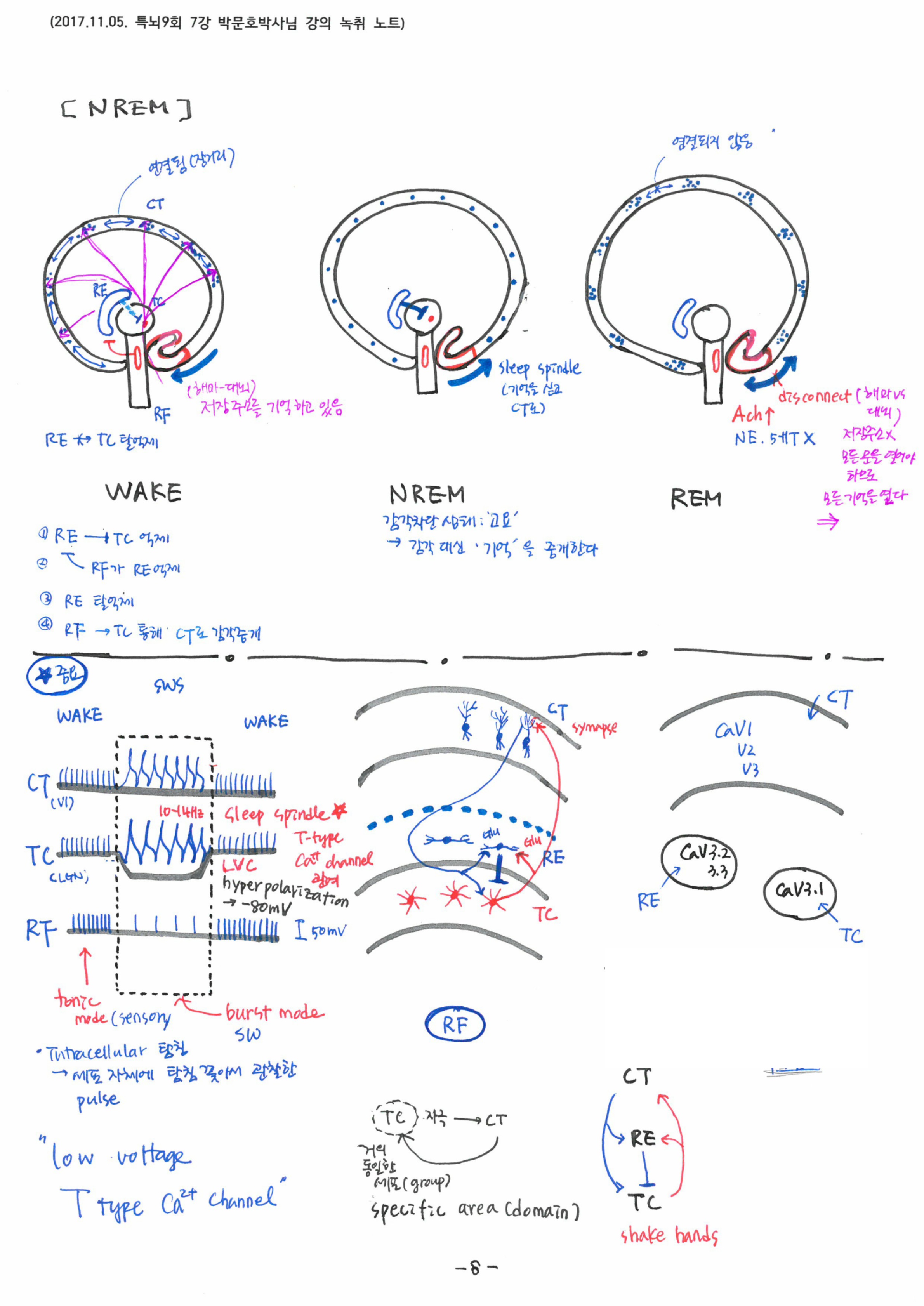
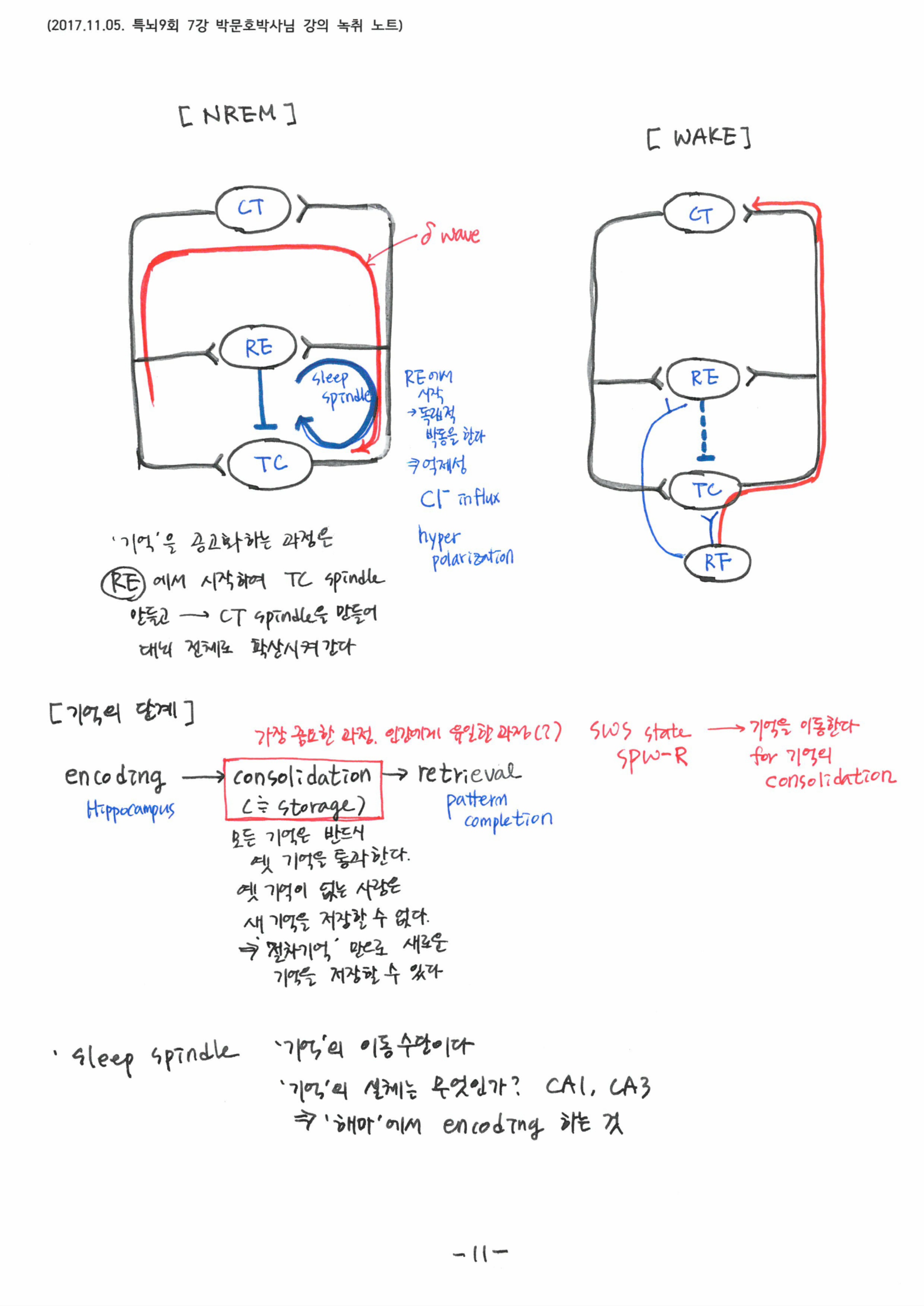
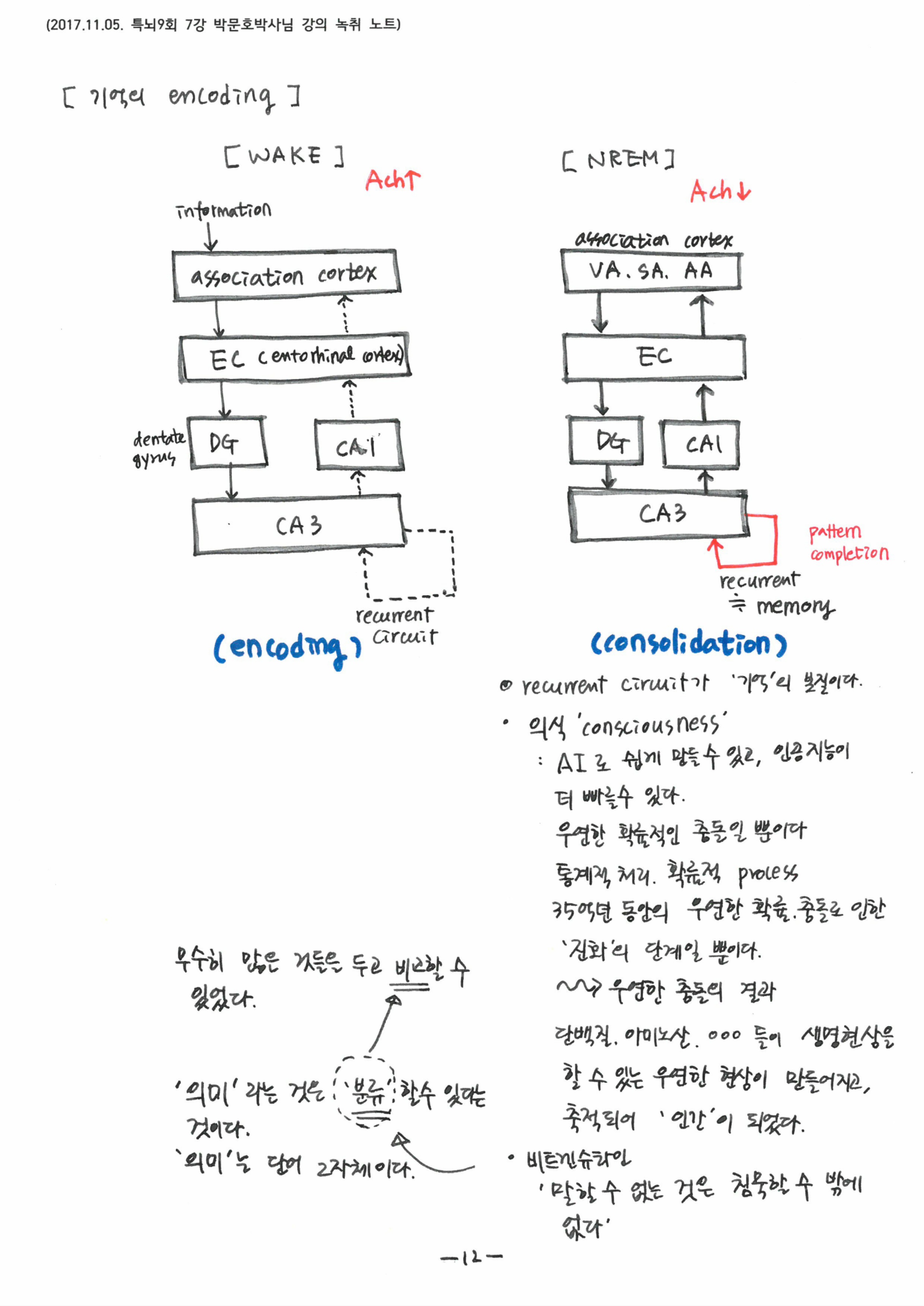
7강에서는 ‘잠’의 실체와 이것이 우리의 ‘기억’과 어떤 연관성이 있는지를 살펴봄으로써 왜 우리가 하루 중 거의 1/3~1/4에 해당하는 시간동안 잠을 자야하는 이유를 배웠습니다. 잠자는 동안 각성 - NREM - REM - 각성으로 이어지는 비가역적인 순서가 있다는 것과 각 단계별로 나타나는 특징적인 뇌파와 연결지어, 단계별로 대뇌 속에서 어떻게 기억이 만들어지고, 공고화되는지를 배웠습니다.
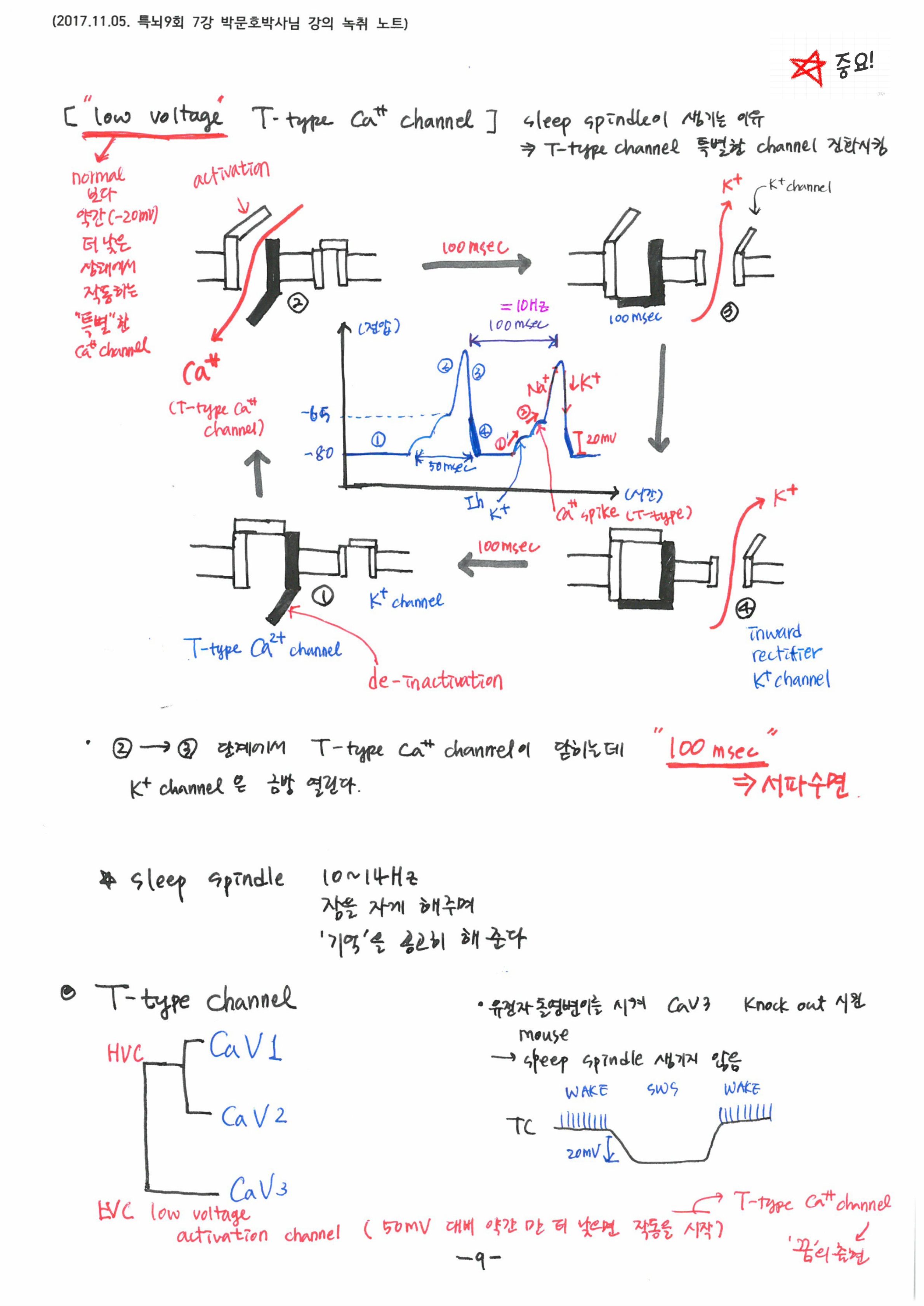
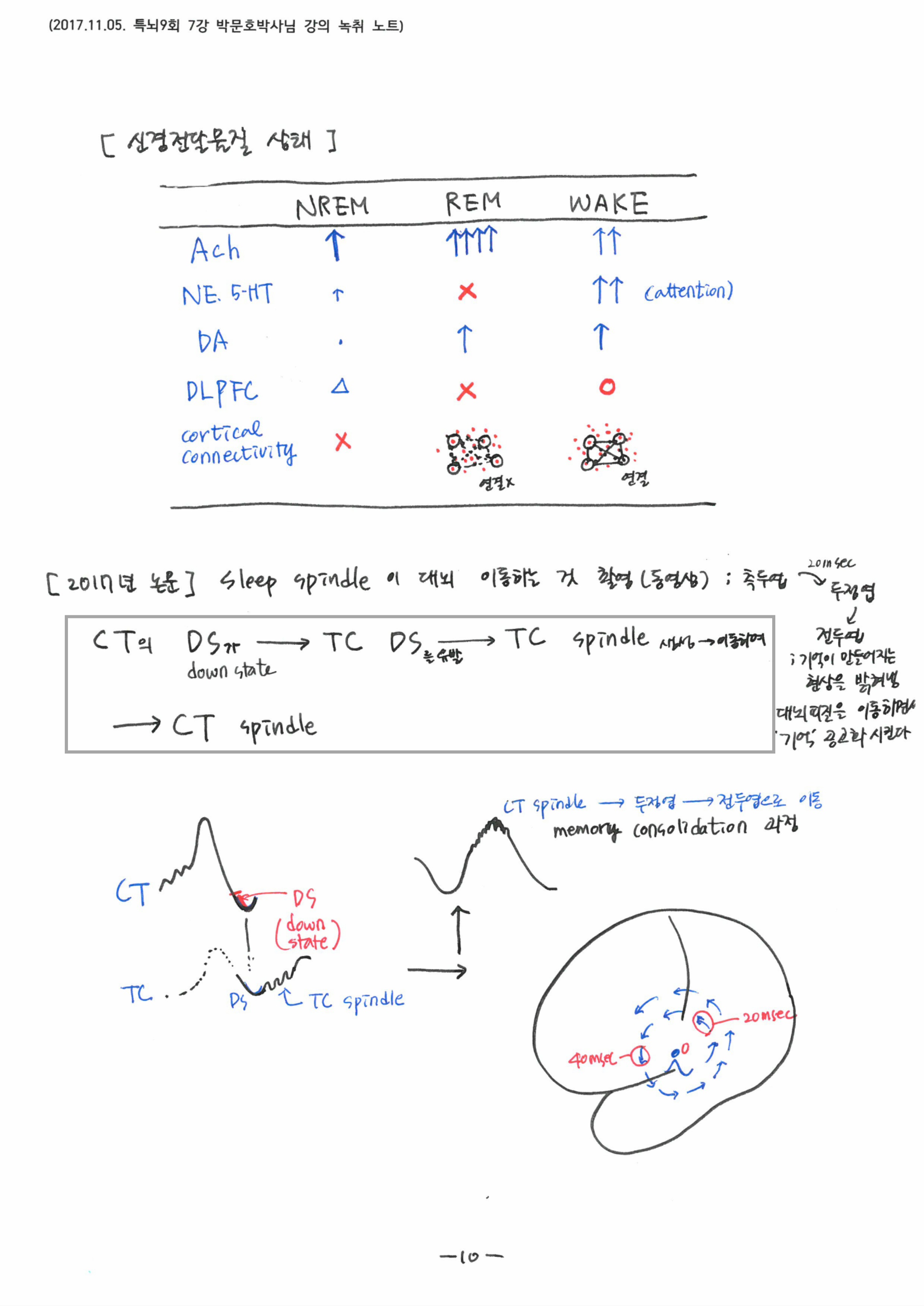
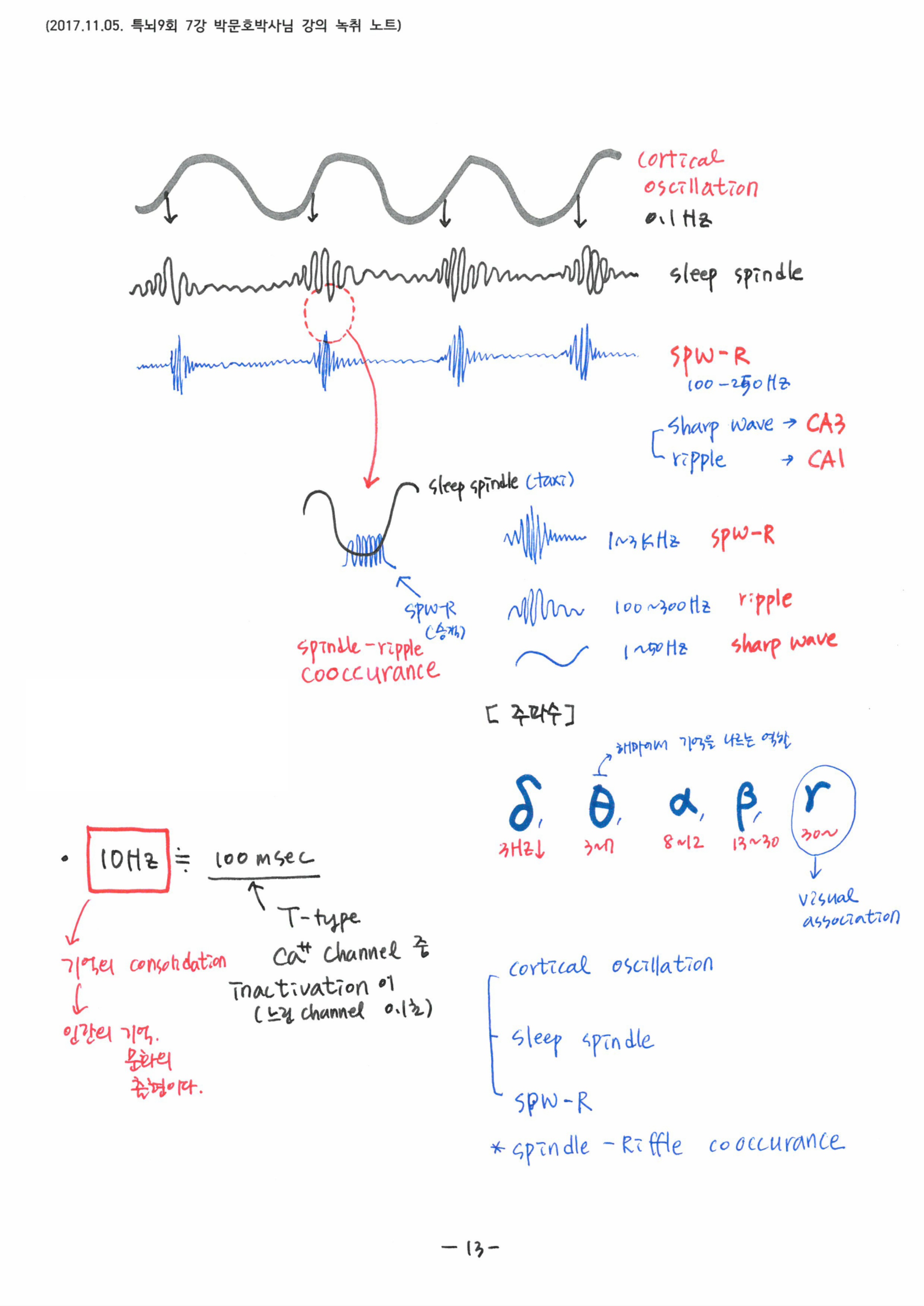
보통의 활성전압과는 다른 특별한 파형의 뇌파를 만드는데 결정적인 역할을 하는 low voltage T-type Ca2+ channel의 작용기전을 통해 생명도, 죽음도 칼슘이 결정적이라는 것을 다시 한번 살펴보았고, 깨어있는 시간동안 입력된 감각정보들이 서파수면동안 인코딩되며, 뇌파 측정결과로 확인된 2017년 최신 논문 내용까지 세밀하게 배웠습니다.
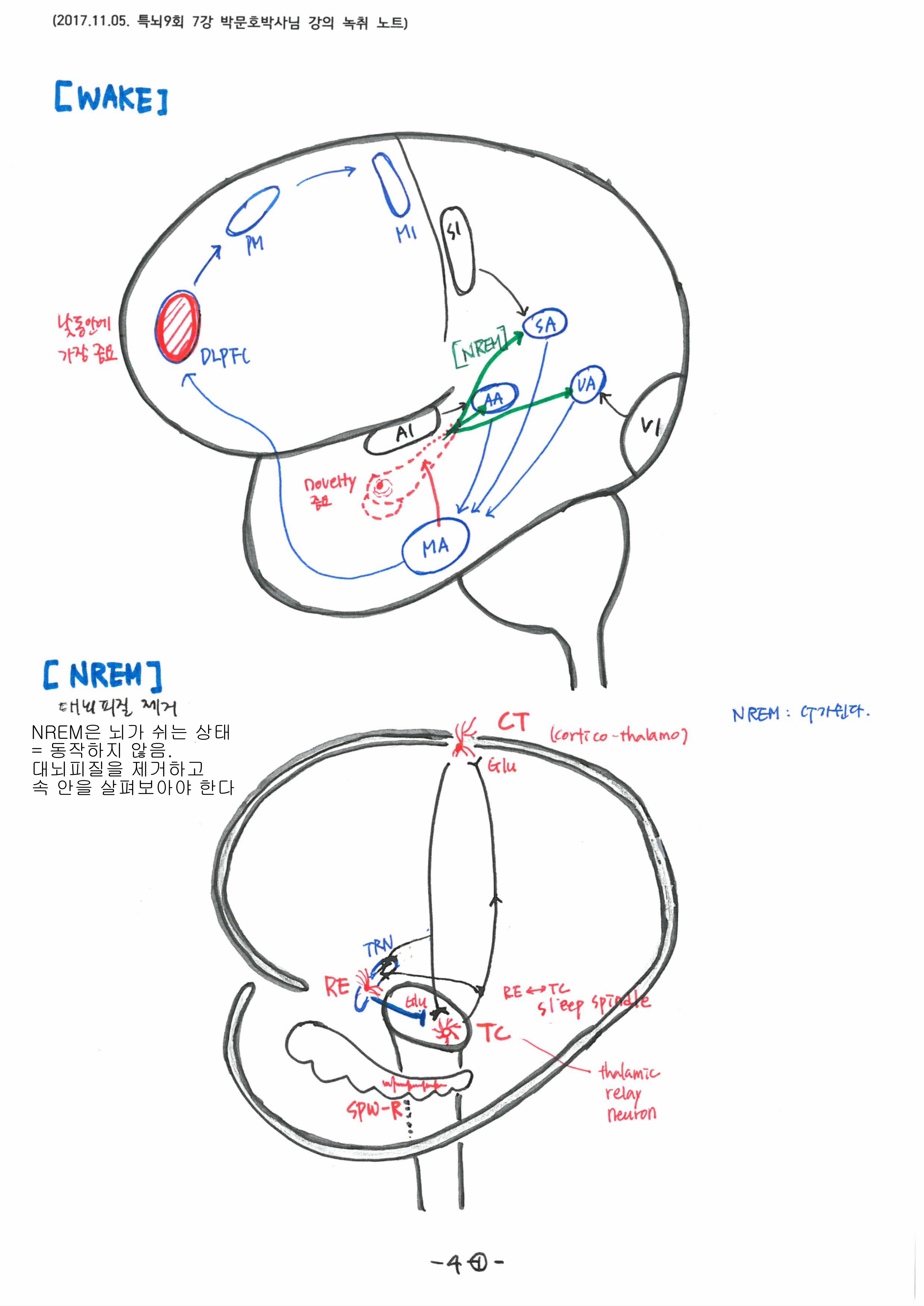
7강의 핵심 키워드는 ‘Sleep spindle & SPW-R’, ‘low voltage T-type Ca2+channel’ 이었고, 각성과 NREM, REM의 중에서 NREM을 가장 주목해야 한다고 강조하셨습니다.
첨부 : 특별한 뇌과학-제7강. 꿈과 기억





- 20171105_9뇌7강.pdf (7.27MB)(524)
- A78940DBC881280291F20E6C7B285F23_1.jpg (497.6KB)(36)
- A78940DBC881280291F20E6C7B285F23_2.jpg (482.0KB)(61)
- A78940DBC881280291F20E6C7B285F23_3.jpg (691.4KB)(52)
- A78940DBC881280291F20E6C7B285F23_4.jpg (657.6KB)(36)
- A78940DBC881280291F20E6C7B285F23_5.jpg (825.9KB)(45)
- A78940DBC881280291F20E6C7B285F23_6.jpg (782.7KB)(36)
- A78940DBC881280291F20E6C7B285F23_7.jpg (689.2KB)(44)
- A78940DBC881280291F20E6C7B285F23_8.jpg (792.8KB)(51)
- A78940DBC881280291F20E6C7B285F23_9.jpg (898.8KB)(58)
- A78940DBC881280291F20E6C7B285F23_10.jpg (767.7KB)(35)
- A78940DBC881280291F20E6C7B285F23_11.jpg (840.1KB)(38)
- A78940DBC881280291F20E6C7B285F23_12.jpg (548.8KB)(37)
- A78940DBC881280291F20E6C7B285F23_13.jpg (632.1KB)(43)
- A78940DBC881280291F20E6C7B285F23_14.jpg (697.4KB)(57)
- A78940DBC881280291F20E6C7B285F23_15.jpg (597.8KB)(41)

low voltage T-type Ca2+ channel의 전압 변화와 관련해서
일반적인 파형대비 (tonic) 서파수면시 나타나는 burst 파형에 대한 설명 (A)과
burst 파형을 만드는데 각 단계에서 영향을 주는 요인 설명 (B)
thalamus에서 Cav3.1을 knockout 시킨 mouse에서 burst 파형이 나타나지 않음을 보여주는 설명 (C) 참조합니다.
http://physrev.physiology.org/content/83/1/117
Fig. 2.
Low-threshold Ca2+ spikes generate burst firing.A: many neurons can generate two distinct patterns of action potential firing in response to a depolarizing stimulus. Regular, or tonic, firing is elicited when the neuron is depolarized from a resting membrane potential near −55 mV. In contrast, when the membrane potential is below −70 mV, the same depolarizing stimulus triggers a high-frequency burst of action potentials. [From Huguenard JR. Low-voltage-activated (T-type) calcium-channel genes identified.Trends Neurosci 21: 451–452, 1998, with permission from Elsevier Science.] B: a representative example of currents that generate burst firing. Depolarization of the plasma membrane by hyperpolarization-activated current (I h) leads to activation of T-type currents (I T), and a second phase of depolarization called the low-threshold Ca2+ spike. Riding on top of the low-threshold Ca2+ spike are a burst of Na+spikes mediated by fast voltage-gated Na+ channels. High-threshold Ca2+ and K+ currents can also be activated by the low-threshold calcium spikes. Ca2+ entry during the burst leads to activation of Ca2+-activated K+currents, which in combination with voltage-gated K+channels repolarize the membrane. (From Bal T and McCormick DA. Synchronized oscillations in the inferior olive are controlled by the hyperpolarization-activated cation currentI h . J Neurophysiol 77: 3145–3156, 1997.) C: thalamic neurons of transgenic mice lacking expression of Cav3.1 do not fire bursts. Current-clamp recordings are from neurons held at −60, −70, or −80 mV, then depolarized or hyperpolarized by current injections of varying magnitudes as indicated below the set of traces. When the resting membrane potential is −60 mV, a depolarizing stimulus triggers tonic firing in both wild-type (+/+) and transgenic (−/−) animals. When the membrane potential (V m) is lowered to −70 mV, a hyperpolarizing stimulus triggers burst firing in neurons from wild-type, but not transgenic animals. When the resting membrane potential is −80 mV, a depolarizing stimulus only triggers burst firing in neurons from wild-type animals. (From Kim D, Song I, Keum S, Lee T, Jeong MJ, Kim SS, McEnery MW, and Shin HS. Lack of the burst firing of thalamocortical relay neurons and resistance to absence seizures in mice lacking α1G T-type Ca2+ channels. Neuron 31: 35–45, 2001, with permission from Elsevier Science.)